Postulado de estado: El estado de
un sistema comprensible simple se especifica por completo mediante dos
propiedades intensivas independientes.
Presión y Temperatura no pueden
ser dos propiedades intensivas
Temperatura y Volumen son dos
propiedades intensivas independientes
-
Un ciclo es cuando el estado inicial y el estado final
es el mismo
-
Proceso es la trayectoria del Estado 1 al Estado 2
Proceso de cuasi estático o de cuasi equilibrio
Quasiequilibrium
Compresión
lenta
Compresión Rápida
-
Cuando la temperatura permanece constante se le llama
proceso Isotérmico.
-
Cuando el volumen permanece constante se le llama
proceso Isocorico.
-
Cuando la presión permanece constante se le llama
proceso Isobático.
Si el recipiente esta abierto
5.-
Vapor Sobrecalentado
T°
Q m
Q=mc T° (FINITA)
Q=n Mc
Mc=C (testado= relacion con molar)
EENTRADA-ESALIDA= ESISTEMA(KJ) energía interna, energía cinetica, energía potencial.
Q-W= U FORMA FINITA










Balance de masa y energía en sistemas abiertos
Diagrama de P-V(Presion-Volumen)
Un fluido es un conjunto de moléculas
que se ordenan aleatoriamente y se mantienen juntas a partir de fuerzas
cohesivas débiles y fuerzas que ejercen las paredes de un contenedor.
Presión solo se utiliza para los
fluidos
Un fluido es puede ser de forma liquida o gaseoso y este
carece de rigidez y elasticidad, este puede tomar la forma de su recipiente.
El colchón de una cama de agua mide 2m de largo y 2m de
ancho y 30cm de profundidad.
Encuentre la presión que ejerce el agua sobre el suelo
cuando la cama de agua descansa en su posición normal. Suponiendo que toda la
superficie inferior de la cama tiene contacto con el suelo.
Presión que se determina en cierto punto se llama presión
absoluta
- Variación de la
presión con la profundidad.
La presión depende de la densidad del fluido y de la
profundidad
Ejemplo 2: La presión absoluta en agua a una profundidad de
5m es de 145 kPa. Determine: a) la presión atmosférica local, b) la presión
absoluta a una profundidad de 5m en un líquido cuya densidad relativa es de
0.85 en el mismo lugar.
Ley de Pascal
Un cambio en la presión aplicada a un fluido se transmite
sin disminución a todos los puntos del fluido y a las paredes del contenedor.
Ejemplo 3: En un elevador de automóviles en una estación de
servicio, el aire comprimido ejerce una fuerza sobre un pequeño pistón que
tiene una sección transversal circular y un radio de 5.0cm. Esta presión se
transmite mediante un líquido a un pistón que tiene un radio de 15.0cm. ¿Qué
fuerza debe ejercer el aire comprimido para elevar un automóvil que pesa 13300N?
¿Que presión de aire produce esta fuerza?
Manómetros (medidores
de presión)
El agua en un recipiente se
presuriza con aire y la presión se mide por medio de un manómetro de varios
fluidos. El recipiente se localiza en una montaña a una altitud de 1400m donde
la presión atmosférica es 85.6 kPa. Determine la presión del aire en el
recipiente si h1=0.1m, h2=0.2m y h3=0.35m. Tome
las densidades del agua, aceite y mercurio iguales a 1000 kg/m3, 850
kg/m3 y 13600 kg/m3, respectivamente.
La presión manométrica en el
tanque de la figura es 80kPa. Calcule la altura diferencial h de la columna de mercurio.
Agua
dulce y de mar fluyen en líneas paralelas y horizontales orientadas entre si
mediante un manómetro de tuvo de doble U. Determine la diferencia de presión
entre las dos tuberías considerando la densidad del agua de mar a este punto es
de 1035 Kg/m3 ¿Se puede ignorar la columna de aire en el análisis?
Barómetro
El barometro basico se puede
utilizar para medir la altura de un edificio. Si las lecturas barometricas en
la parte superior y en la base del edificio son 730 y 755mmHg respectivamente,
determine la altura del edificio. Tome las densidades del aire y del mercurio
como 1.18 kg/m3 y 13600 kg/m3, respectivamente
Ley Cero de la Termodinámica (R. H. Fowler, 1931)
Cuando dos objetos (A y B) están con otro tercero (C) se
dice que (A y B) están en equilibrio entre si.
T1>T2
|
||||||
T1(ºC)
|
T2(ºC)
|
ΔT(ºC)
|
ΔT(ºF)
|
ΔT(K)
|
ΔT(R)
|
|
20
|
15
|
-5
|
||||
T(F)
|
68
|
59
|
-9
|
|||
T(K)
|
293
|
288
|
-5
|
|||
T(R)
|
528
|
519
|
-9
|
|||
ΔT(ºF)=1,8ΔT(ºC)
|
||||||
ΔT(R)=1,8ΔT(K)
|
||||||
Una campana de 250mm de diámetro se coloca sobre una
superficie plana y el aire se evacua hasta un vacío de 700mmHg. El barómetro
local da una lectura de 760mm. Encuentre la presión absoluta dentro de la
campana.
Pvacio=(13600
kg/m3)(9.81 m/s2)(0.7 m )=93391.2 Pa
Patm=(13600
kg/m3)(9.81 m/s2)(0.76 m )=101.39 Pa
Pabs=
Patm- Pvacio=8.006 kPa
Pvacio=700mmHg → 101.325
kPa Mg.
hHg=760mm → Patm==(13600 kg/m3)(9.81
m/s2)(0.76 m )
Calcule la presión en un cilindro de 200mm de diámetro como
se muestra en la figura el resorte se comprime 40 cm .
F=-Kx
F=-(-2kN/m)(.4m)=0.8kN
F=mg
F=((40kg)(9.81m/s2)=392.4N
P=F/A
P= (800N+392.4N)/ π(0.1m)2 = 37955.27 Pa
FI-mg-FS-FR=0
FI=PIA FS=PatmA
PI=
(mg+Patm+Kx)/A
PI=
[(40kg)(9.81m/s2)(1kN/1000N)]+[(101.325kPa)( π(0.1m)2)]+[(2kN/m)(0.4m)]
π(0.1m)2
PI=139kPa
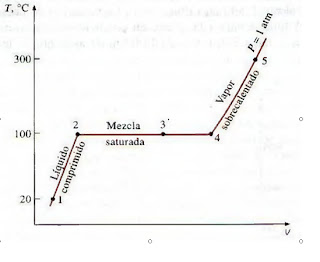
Unidad II: Propiedad de las sustancias puras.
Sustancia pura: tiene 5 fases.
1.- Líquido
Comprimido
2.- Líquido
Saturado
3.- Mezcla
Saturada
4.- Vapor
Saturado
Ejemplo: Un recipiente rígido condene 50 kg de agua saturada a 90 ºC . Determine la presión
en el recipiente y el volumen del mismo.
Liquido
saturado
T=90ºC
m=50kg
agua (tabla A-4)
P=Psat@90ºC=70.183 kPa Presión
dentro del recipiente
V=V/m
V=Vf@90ºC(m)
V=0.001036 m3/kg(50kg)
V=0.0518m3 Volumen
“ESTADO
LIQUIDO SATURADO – VAPOR SATURADO”
Ufg = Ug – Uf
Hfg = hg – hf
Hfg= entalpia de vaporización
EJEMPLO: Un recipiente rígido contiene 50kg de agua saturada a 90 ˚C. Determine la presión en el recipiente y el
volumen del mismo.
DATOS:
Agua liquido saturado ….temperatura 90˚C P = P sat. A 90˚C = 70.183 kPa
√ = V/m V
= √ m
= (50kg) ( 0.001036 )
)
V =
0.0518 
Ejemplo:
V = Vf+ Vp √ = V/m V
= √ m
M total √ promedio = mf Df + mg Dg
√ prom. = (m f / m total) vf + X Dg m f = m total = m g
√ prom. = ( 1- x) Vf + X Vg
√ prom. = Vf + X Vfg gral.
V =
Vf + X V fg y = Yf+X
Yfg X = (y – yf/yfg)
Un recipient de 80 lt.
contiene 4kg de refrigerante 134a a una presion de 160 kPa . Determine:
a)
La temperatura
b)
La calidad
c)
Entalpia del refrigerante
d)
El volumen que ocupa la fase de vapor
DATOS:
Fase
¿? m = 4kg P = 160 kPa
V = 80 lt.
√ = V/m
√ = (80 lt ( 0.001 / 1L)) /
4kg √ = 0.02
/ 1L)) /
4kg √ = 0.02
Tabla
A-12 Vf = 0.0007437 
a)
-15.60 ˚C Vg = 0.12348 
b)
X= (V
– Vf) / ( Vfg) à = ( 0.02 – 0.0007437) /
(0.12348 – 0.0007437)
X= 0.157
a) H = hf + x hfg hfg = 31.21 KJ / Kg
Por lo tanto h = (31.21) + ( 0.157) (209.90) X = 0.157
hfg = 209.90 KJ / Kg
RESULTADO: h
= 64.1643 KJ / Kg
b)
Vg = mg √g à mg = x m total por lo tanto:
Vg
= (0.157) (4Kg) (0.12348 m3 / Kg)
= 0.0775 m3 = 77.5 lts.
-VAPOR SOBRECALENTADO-
P < Psat a una T dada
T > Tsat a una P dada
V > Vg a una T o P dada
U > Ug a una T o P dada
h > hg a una T o P dada
-LIQUIDO COMPRIMIDO-
P > Psat a una T dada
T < Tsat a una P dada
V < Vf a una P o T dada
u < Uf a una P o T dada
h < hf a una P o T dada
Aproximada a liquido
saturada
Y = Yf a T Tablas A - 4
A - 4 E A - 11 A - 11E
Y = V/h
Un vapor a 120
bar tiene un volumen especifico = 0.01721 m3 / Kg , encuentra la Temperatura
entalpia y energía interna.
DATOS:
Fase ¿?
P 120 bar = 12 MPa √
= 0.01721 m3 / Kg
Tabla A – 5 Vf a 12MPa = 0.001526 m3 / Kg
Vg a 12MPa = 0.014264 m3
/ Kg
V > Vg >> Vapor sobrecalentado
Ahora … Tabla A –
6
X = ((0.001566 – 0.001526) / 13 – 12 )
(12.5- 12) + 0.001526
X =
0.001546
INTERPOLACION GENERAL
a1 b1
a b
b = [(b2 –b1) / (a2 – a1)] (a
- a1) + b1
a2 b2
por lo tanto… Vf = 0.001546 m3 / Kg
T =
[12846.86536] – [0.01721 – 0.0016138] + 350
T =
363.8 ˚C
P = mg / A
MODELO
DE GAS IDEAL
è Boyle – Mariotte
V α 1/P ( n, T constante) donde n = numero de moles
è CHARLES
V α T ( n, P ctte)
è AVOGADRO
V α nT / P V = RnT / P
ECUACION
del GAS IDEAL PV =
nRu T n = m/M
Ru = ctte universal de los gases
PV = RT
Ru = ( 1 atm) ( 22.414) / (1 mol) (273.15) = 0.08206 { L * atm / mol * K}
Ru = {…}
è { 0.08206 (L*atm
/ mol*K)
è
8.114 (Pa*m3/mol*K)
è 62.4 (mm Hg /
mol* K)
PV = RT à P V/M = RT densidad
= P / RT
1) n,T P1V1
= P2 V2
2) n,P V1 / T1 = V2 / T2 ””ECUACION GENERAL DE LOS GASES””
3) n,V P1 /
T1 = P2 / T2
[(P1 * V1) / T1] = [(P2 * V2) / T2]
Factor de comprensibilidad
Z = PV / RT
z = √ / √ ideal Tr = T / Ter
√r = (V
presion critica / R tempretatura critica)
Por un tubo pasa el gas de dióxido de carbono a 3 Mpa y 500
K, el flujo constante de 0.4Kmol por segundo, Determine a) las tasas de flujo
de volumen y de masa y la densidad del dióxido de carbono en dicho estado. Si
el dióxido de carbono se enfria a presión constate al pasar por el tubo de modo
que su temperatura baje a 450°K a la salida; determine b) la tasa de flujo
volumétrico a la salida del tubo.
P=3Mpa
T=500K
R=.1889KJ/Kg.K
n=0.4Kmol.seg
M=44.01Kg/Kmol
Δ=(300Kpa)/(0.1889Kpa.m³/Kg)(500K)=
31.762m³/Kg
n=m/M m=nM
m=(0.4Kmol.seg)(44.01Kg/Kmol)
m=17.604Kg.seg
III Primera
ley de la termodinámica
3.1 Trabajo
de frontera móvil
W=FdcosΘ
∫W=FdscosΘ
=Fds
P=F/A
F=PA
∫w =∫Pdv
Isocorico
Wb=∫Pdv
Isobarico
A=BxH=(V₂-V₁)P
Wb=P(V₂-V₁)
V₂>V₁=Wb>0
↓
+ el sistema
realiza trabajo.
V₁>V₂=Wb<0 → -
Se realizo trabajo sobre el sistema.
Ejemplo:
Al principio un dispositivo de cilindro embolo contiene .4m³
de aire a 100 Kpa y 80°C. se comprime el aire a 0.3m³ de tal manera que la
temperatura dentro del cilindro permanece constante. Determine el trabajo hecho
durante este proceso.
Wb=∫Pdv
P=F(V)
Aire como gas ideal
PV=NRuT
P=(nRuT)/V
Wb=∫nRuT
dv/v
Wb=nRuT Ln
V|V₂ - V₁
n=(PV₂)
/RuT
(P₁V
RuT)/RuT, Ln
(V₂/V₁)
Wb={100KPa}{0.4m³}
Ln (0.1m³/0.4m³) KJ
Wb= -55.45KJ.
CALOR
T°
Q m
Material, calor especifico (capacidad para amacenar entre mayor es peor
conductor)
Q=mc T° (FINITA)
∫Q=mcdT° (INFINITESIMAL)
Q=mc T (J) n=m/M m=Nm
C=Q/(m T)
=J/Kg°C= J/ Kg°K
Q=n Mc
Mc=C (testado= relacion con molar)
Capacidad
calirifica molar.
Q=nC T
J/Mol°C Ó J/Mol°k
¿cambios de fase? Calor latente.
Q=±ml (J)
+ agrega calor
-Pierde calor.
Hielo agua /vapor/ 105°C
-3
Liquido-vapor
Q=mLv
Vapor-iquido Q=-mLv
Solido-iquido Q=mLf liquido-solido Q=-mLf
Una olla gruesa de cobre de 2kg. Incluyendo su tapa esta a
una temperatura de 150°C, usted vierte en ella 0.1KG de agua a 25°C y
rápidamente tapa la olla para que no escape el vapor. Calcule la temperatura
final del vapor y su contenido y determinar la fase liquido gas del agua.
Suponga que no se pierde calor al entorno.
Ccobre= 390J/Kg.K -Qco=Qagua
Cagua=4190J/Kg/K
Lv= 2.256 x10⁶J/Kg
Suponga que:
i)
Nada del agu hierve t la temperatura será menor
a 100°C
ii)
Una parte de agua hierve a 100°C
iii)
El agua hierve y se evapora T=100°C o mas.
i)mal por que T > 100°C
-mcuCcu(T-Tcu)=maca(T-Ta)
(-2Kg)(390J/Kg.K)(T-180)
°C= (0.1Kg)(4190J/kg°C)(T-25°C)
-780J/K(T-180)°C=419J/°C(T-25)
°C
(-780J/K)/(419J/C) (T-180)°C= (T-25) °C
1.86(T-180) °C=(T-25) °C
1.86(T-180) °C-(T-25) °C=0
T=106.32°C
-mcuCu (T-Tcu)=maCa(T-Ta)+XmaLv
(-2Kg)(390J/Kg.K)(50°C)= (0.1Kg)(4190J/kg°C)+x(0.1Kg)(2.256X10⁶J/Kg)
39000=31425+2.256X10⁶
X=0.034
Mv=(0.034)(100g)=3.4g
T=100°C
En cierta estufa de gasolina para acampar, 30 de a energía
liberada al quemar el combustible calienta el agua de la olla en la estufa. Si
calentamos un litro de agua de 20°C a 100°C y evaporamos .25g de ella. ¿cuanta
gasolina habremos quemado?. 1 g de gasolina libera 46000 J.
M=1lt.=1Kg.
Q=46000J
T₁=20°C
T₂=100°C
C=4190 J/Kg.k
Q=mc
T=(1kg)(4190J/Kg.k)(100-20) °C
Q=325200J
Liquido vapor
Q=mLv=(.256X10⁶J/Kg)=564000j
1g gasolina=2997333.333J
m=0.0651594 kg
ρ=m/v V=m/ρ
v=.0651594kg/120kg/m³=9.04941X10⁻⁵m³=.09049=90.5 ml
Balance de energía para sistemas cerrados
EENTRADA-ESALIDA= ESISTEMA(KJ) energía interna, energía cinetica, energía potencial.
Transformacion neta de energía y trabajo
Q-W= U FORMA FINITA
∫Q-∫W=dv FORMA
INFINITESIMAL
Se condensa isotérmicamente vapor sasturado a 200°C hasta
liquido saturado en un dispositivo de cilindro embolo. Calcule el calor
transferido y el trabajo efectuado en este proceso en KJ/Kg.
1
2
Vapor saturado (Vg@200°C=.12721m³/kg) liquido saturado( Uf@200°C=.001157m³/kg)
¿Q y W?
BALANCE DE ENERGIA
Wb-Q= U
Wb –Q=U₂-U₁
Uf@200°C UG@200°C
P₁=P₂=1554.9KPa
Wb=∫Pdv
Wb=Mp(Vf-Vg)
Wb/m=1554.9KPa(.001157-0.12721)m³/Kg
Wb=-196KJ/Kg
Wb-q=U₂-U₁
Q= Wb-u₂+U₁= 196KJ/Kg
- 850.46KJ/Kg + 2594.2KJ/Kg
1940 KJ/Kg
Un recipiente rigido de 1ft³ contiene refrigerante
134-aoriginalmente a -20°F Y 27.7% de calidad. A continuación se calienta el
refrigerante hasta que su temperatura es 100°F calcule la transferencia de
calor necesaria para este proceso.
Un dispositivo de cilindro embolo se expande 25g de vapor de
agua saturado a una presión constante de 300Kpa. Se enciende un calentador de
resistencia eléctrica dentro de cilindro y pasa
una corriente de .2A durante 5 min. Desde una fuente de 120V. al mismo
tiempo ocurre una perdida de calor de 3.7 J. determine la temperatura final del
vapor.
Un dispositivo que consta de un cilindro embolo contiene
inicialmente .5m³ de gas nitrógeno a 400pa y 27°C .dentro del dispositivo se
enciende un calentador eléctrico con el cual pasa una corriente de 2 amperes
durante 5 minutos, desde una fuente de 120v. el nitrógeno se expande a presión
constante y ocurre una perdida de calor de 2800 J durante el proceso determine
la temperatura final de nitrógeno.
La salida de potencia de una turbina de vapor adiabatica
es 5MWmientras que las condiciones de entrada y salida son como se indica en la
figura
a)determine el trabajo hecho por unidad de masa del vapor
de agua que fluye por la turbina
b)
calcule el flujo masico de vapor
Se tiene una regadera ordinaria
donde se mezclan agua caliente a 140°F y fría a 50°F.se desea suministrar una
corriente estable de agua caliente a 110°F.determine la relación de los flujos
masicos de agua caliente y fría. Suponga que las paredes de calor desde la
cámara de mezclado son insignificantes y que el mezclado ocurre a una presión
de 20Psia.
Refrigerante 134-a se va a
enfriar con agua en un condensador. El refrigerante entra al dispositivo con un
flujo masico de 6Kg.m a 1 Mpa y 70°C, y sale a 35°C. e agua de enfriamiento
entra a 300Kpa y 15°C y sale a 25°C. sin considerar las caídas de presión
determine a)el flujo masico de agua de enfriamiento requerido b) la tasa de
transferencia de calor desde el refrigerante hacia el agua.
Balance de masa y energía en sistemas abiertos
Principio
de la conservación de la masa
Flujo
estacionario este es cuando no cambia con respecto al tiempo
Energia
o trabajo de flujo
Wflujo=FL=PAL=PV
[kJ]
Wflujo=PV [kJ/kg]
Energia
total de un flujo en movimiento
e=u+Vel2/2+gz [kJ/kg]
θ= e+PV [kJ/kg]
θ=
u+Vel2/2+gz+PV
θ=h+ Vel2/2+gz [kJ/kg]
Cantidad de
energia transportada
Emasa=mθ [kJ]
Tasa de
energia transportada
Instrumento
|
Descripción
|
Transferencia
de calor
|
Trabajo
|
Δep
|
Δec
|
Toberas Aceleradoras
|
incrementa la velocidad de un
fluido a expensas de la presión
|
≈0
|
0
|
~=0
|
≠0
|
Difusor
|
incrementa la presión de
un fluido al desacelerarlo
|
≈0
|
0
|
~=0
|
≠0
|
Turbinas
|
el fluido pesa por esta y girar
la turbina produce trabajo
|
≈0
|
EW
|
~=0
|
~=0
|
Compresor
|
incrementa la presión de
un fluido
|
≈0
|
EW
|
~=0
|
~=0
|
Válvula de Estrangulamiento
|
Dispositivo que restringe el fluido con el flujo adiabático
|
0
|
~=0
|
~=0
|
|
Cámaras de mezclado
|
Sección de mezclado de flujos
|
~=0
|
0
|
~=0
|
~=0
|
Intercambiadores
de calor
|
Dos
corrientes de flujo
intercambian
calor sin mezclado
|
0
|
~=0
|
~=0
|
Flujo estacionario
Un difusor de un motor de propulcion entra de forma estacionaria
aire a 10ºC
y 80kPa con una velocidad de 200m/s. El area de entrada al difusor es 0.4 m2 . El aire
que sale del difusor con una velocidad que es muy pequeña comparada con la
velocidad de entrada. Determine
a) El
flujo masico del aire
b) La
temperatura del aire que sale del difusor